Planten hebben groene bladeren. Dat groen wordt veroorzaakt door zogenaamde bladgroenkorrels. Die korrels kunnen het energie van het licht gebruiken om CO2 om te zetten in glucose (een soort suiker) en daarmee zetmeel, vezels en andere koolhydraten maken. Dit proces wordt fotosynthese genoemd. Dat kunnen alleen groene planten. De mens heeft dus planten nodig om aan een glucosebron te komen want glucose is een hele belangrijke bouwstof, niet alleen voor de plant maar ook voor ons.
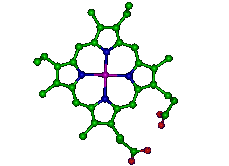
Naast het bekende chlorofyl, dat in eerste instantie het licht opvangt, zit er in bladgroenkorrels het zogenaamde cytochroom. Chlorofyl en cytochroom lijken qua bouw heel veel op elkaar. Beide molekulen hebben een ringvormige struktuur. Echter, in het chlorofyl zit in het centrum een magnesiumatoom, terwijl er in het cytochroom een ijzeratoom zit. Een ander bekend molekuul dat heel sterk lijkt op het cytochroom is hemoglobine dat het zuurstof in ons bloed bindt en eveneens eveneens een ijzeratoom bevat. Dat cytochroom is belangrijk in het doorgeven van de opgevangen energie uit licht aan andere molekulen.
Gebrek
Gebrek aan ijzer is makkelijk te zien aan de steeds geler wordende toppen van planten. Toevoegen van ijzer heft dit relatief weer snel op, meestal binnen enkele uren. Omdat een plant heel veel bladgroen nodig heeft om te kunnen groeien en omdat de vorm waarin de plant het kan gebruiken snel ongeschikt wordt, heeft het dus ook een vrij grote behoefte aan ijzer.Maar wat is dat voor ijzer dan? IJzer komt op aarde in verschillende vormen voor. Het bekenst is natuurlijk het gewone metaal. In de scheikunde wordt dat aangeduid met Fe. Fe is een afkorting van ferrum dat uit het latijn komt en 'ijzer' betekent. Maar ijzer komt ook in andere vormen voor. Denk maar eens aan roest. Eigenlijk is roest niets anders dan ijzer dat aan de lucht is geoxideerd. IJzer is een reactie aangegaan met zuurstof. Zuurstof wordt weergegeven met een O zodat we roest kunnen opschrijven als Fe2O3. Dat betekent dat er twee atomen ijzer en 3 atomen zuurstof inzitten. Omdat een zuurstofatoom altijd twee elektronen te delen heeft, heeft ijzer in roest er dus blijkbaar 3 tekort. Drie keer twee elektronen over is gelijk aan twee keer drie tekort (3 x 2- = 3 x 3+) zodat het geheel weer neutraal is. In roest heeft ijzer dus drie elektronen tekort en dat wordt opgeschreven als Fe3+.
Nou komt het vervelende. In het hart van het cytochroom moet een Fe2+. Een Fe3+ past niet! Geen probleem, dan neemt de plant maar een Fe2+ op, zou u misschien denken. Maar Fe2+ is een lastpak. Zo gauw als het de kans krijgt wil het Fe3+ worden. Licht en zuurstof bijvoorbeeld zijn al voldoende om het Fe2+ om te laten zetten in Fe3+. Dus als u een ijzersupplement koopt in de winkel zit daar een chelaat bij. Dat chelaat is een fraai molekuul meestal in de vorm van een grote C. Twee van de molekulen kunnen zo een Fe2+ omklemmen zodat er niks mee kan gebeuren. Alleen de plant kan het ijzer er weer uit halen. Fraai toch?
Nu die oude rotten met hun fraaie planten. Ten eerste zat er vroeger meer ijzer in het drinkwater. Nu wordt het zo gezuiverd en steeds meer waterleidingen zijn van plastic dat er nauwelijks meetbare hoeveelheden ijzer in het water blijft. Ten tweede hadden die oude rotten trukjes zoals een oude roestige spijker en rode klei dat onder de planten werden ingegraven. Waar was dat goed voor?
Zoals we zagen kan ijzer met zuurstof uit de lucht reageren tot roest. 2 IJzer en 3 zuurstof oftewel Fe2O3. Maar er bestaat ook een andere vorm van roest: FeO. Dat arme ijzer moet het doen met één zuurstof. Let ook even op de vorm van het ijzer hierin. Zuurstof heeft twee elektronen teveel dus dat Fe heeft er twee tekort: Fe2+ dus! Roest is roodbruin en FeO is zwart. Als het mogelijk is om uit roest een zuurstof te halen dan valt dat roest uiteen in twee FeO molekulen. Maar dat zuurstof zit goed vast. En als zouden we dat er af kunnen halen, als het de kans krijgt neemt het dat weer op om weer gewoon roest te worden.
Door verbranding kan dat ene zuurstof worden weggejaagd. Als dakpannen, gemaakt van klei worden gebakken krijg je rode dakpannen. Maar worden die dakpannen gebakken in een goedafgesloten ruimte dan worden ze zwart! Fe2O3 wordt dan dus FeO. Nou kunnen we moeilijk ons aquarium in een oven zetten maar er is hulp en wel van een bacterie: Pseudomonas. Deze bacterie leeft onder zuurstofarme omstandigheden en kan het Fe3+ omzetten in Fe2+. Een bodem met een open stuctuur geeft zuurstof de mogelijkheid om bij de wortels te komen. Roest blijft dan roest. Klei heeft natuurlijk door zijn kleine deeltjes al de neiging om de bodem vrijwel ondoordringbaar te maken voor zuurstof. In het aquarium hebben we dus een relatief vaste, voor zuurstof ondoordringbare laag nodig om Fe2+ te krijgen dat de planten kunnen gebruiken.
Conclusie
Om koolhydraten te maken heeft een plant ijzer nodig. Dat moet tweewaardig ijzer zijn oftewel Fe2+. Dat ijzer wordt meteen Fe3+ (gewone roest) onder invloed van zuurstof of licht. Aan water toegediend moet het ijzer dus beschermd worden en dat doen we met chelaten. IJzer kan ook in klei worden toegediend. Er moet zich dan wel een laag vormen die verhindert dat er zuurstof in de bodem kan komen. Bacterien zetten dan Fe3+ weer om in bruikbaar Fe2+.
